Надниркові залози: будова та функції
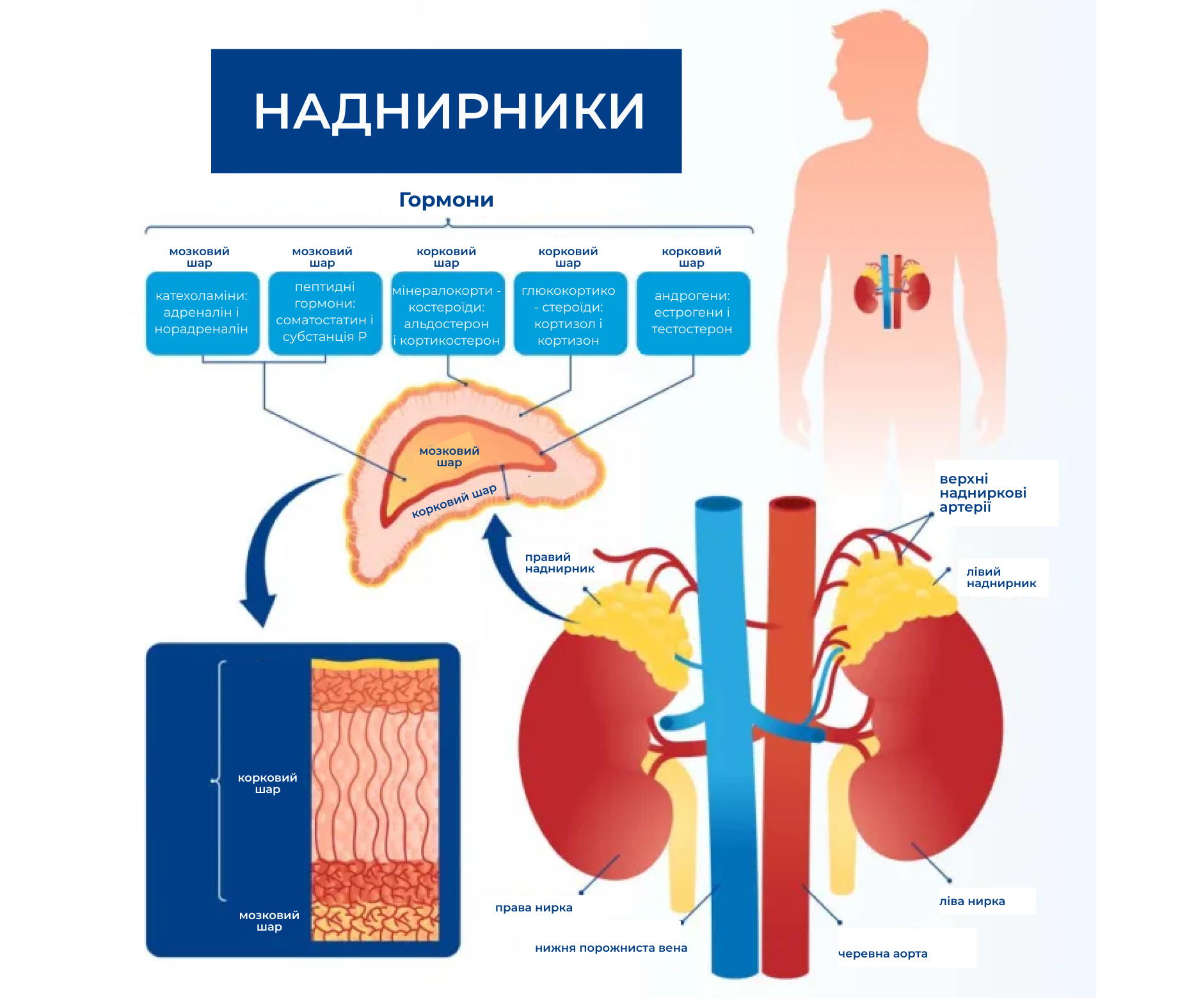
Надниркові залози (наднирники) – два симетричних органи, розташовані заочеревинно над верхніми полюсами нирок, які складаються з двох шарів: кори, яка виділяє стероїдні гормони, і серцевини, яка виділяє катехоламіни.
Надниркові залози відіграють дуже важливу роль в організмі, оскільки гормони, які вони виділяють, дають змогу організму реагувати на фізичні та психічні навантаження.
Реакція організму на зміну умов навколишнього середовища, ситуації фізичного та психічного напруження здебільшого залежить від гормональної реакції гіпоталамо-гіпофізарно-надниркової системи.
Механізм, який регулює секрецію цих гормонів, називають петлею негативного зворотного зв’язку гіпоталамус-гіпофіз-наднирники.
Кортикотропін-рилізинг-гормон (КРГ), що виділяється в гіпоталамусі, регулює секрецію адренокортикотропного гормону (АКТГ) у передній долі гіпофіза (АКТГ перебуває у негативному зворотному зв’язку з КРГ). І навпаки, кору надниркових залоз контролює гіпофіз у відповідь на адренокортикотропний гормон (АКТГ).
Клітини кори надниркових залоз виділяють три основні групи гормонів, кожна з яких виконує певні функції.
- Глюкокортикоїди – які виробляються у середньому шарі кори наднирників, переважно у відповідь на стрес, допомагають контролювати швидкість метаболізму білків, жирів і цукрів (кортизол).
- Мінералокортикоїди – які виробляються у зовнішньому шарі кори наднирників, впливають на артеріальний тиск та регулюють об’єм крові (альдостерон).
- Андрогени – які виробляються у внутрішньому шарі кори наднирників (ретикулярному), контролюють статевий розвиток (DHEA/DHEA-S, андростендіон).
Глюкокортикоїди
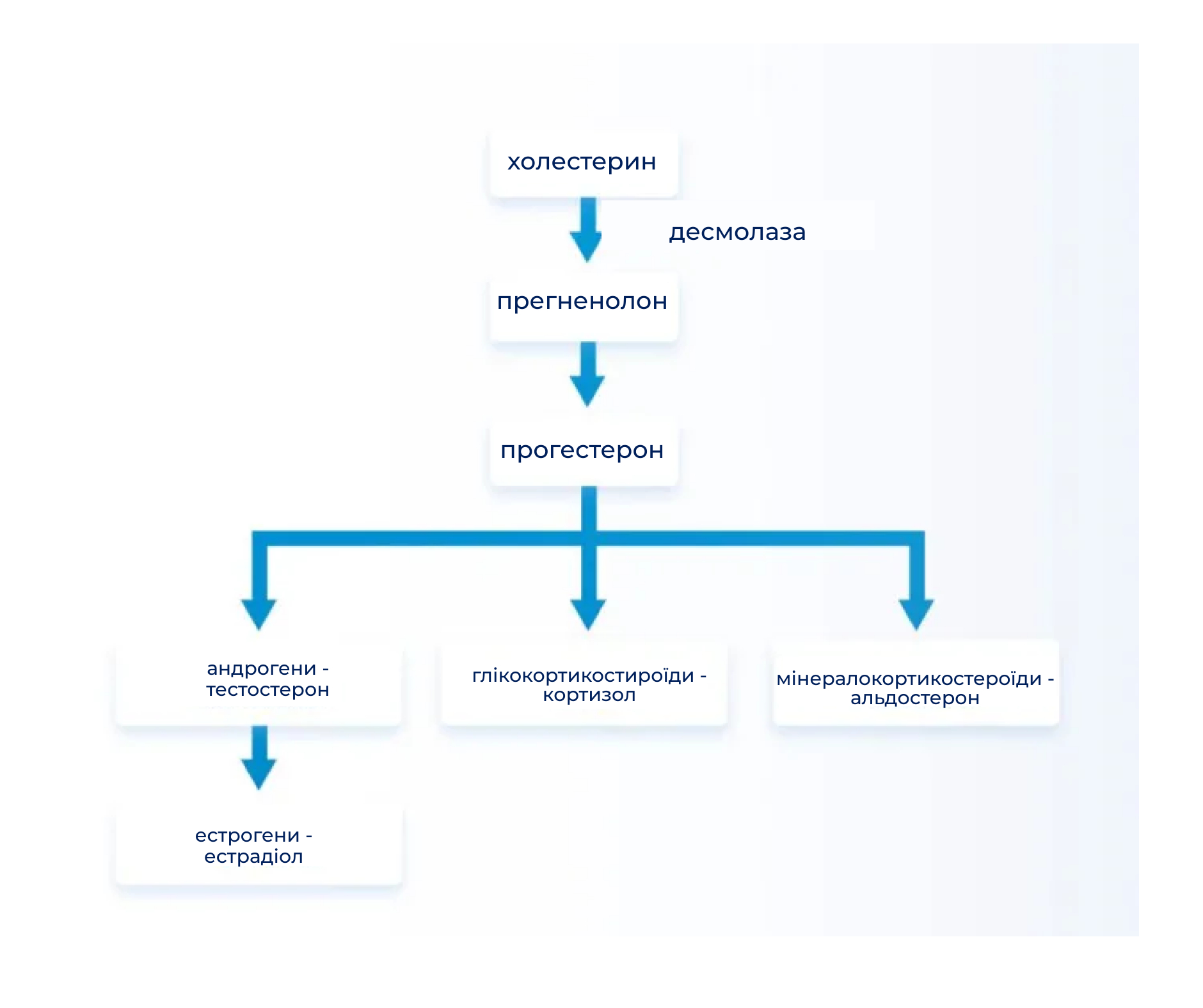
Стероїдні гормони виробляються з холестерину через низку реакцій у мітохондріях і гладкому ендоплазматичному ретикулумі. Холестерин, який надходить з їжею або синтезується у клітинах, зберігається у цитоплазмі клітин, які синтезують стероїди. Усі стероїди мають однакову базову структуру, утворену чотирма кільцями.
Перетворення холестерину в стероїдний гормон проходить у два етапи. Стероїдні гормони виділяються одразу після синтезу.
Мінералокортикоїди
Мінералокортикоїди, які сприяють підтриманню іонного балансу плазми, необхідні для нормальної концентрації натрію й калію та нормального об’єму позаклітинної рідини. Вони підвищують артеріальний тиск, стимулюючи специфічні рецептори у центральній нервовій системі. Основним мінералокортикоїдом є альдостерон.
Aндрогени
Надниркові андрогени синтезуються у сітчастому шарі кори надниркових залоз. Основними андрогенами є андростендіон і дегідроепіандростерон.
Андрогени, які виділяють надниркові залози, мають слабку біологічну дію. У периферичних тканинах вони перетворюються у більш активні андрогени, наприклад тестостерон, у якому, окрім інших, бере участь ароматаза.
Секреція надниркових андрогенів починається ще до повного статевого дозрівання, коли дозріває сітчастий шар і підвищується концентрація дегідроепіандростерону (ДГЕА).
Концентрація ДГЕА і ДГЕА-С тісно пов’язана з віком людини та зростає у віці від 6 до 8 років. Найвищу концентрацію спостерігають у віці близько 25 років, та згодом вона поступово знижується. У віці 80 років концентрація ДГЕА і ДГЕА-С становить 20% від максимального рівня.
У дорослих чоловіків андрогени надниркових залоз становлять лише 5% загальної андрогенної активності, тому вони фізіологічно не значущі. Однак у жінок вони становлять близько 50% загальної андрогенної активності (вони стимулюють розвиток лобкового та пахвового волосся).
У жінок 40–60% циркулюючого тестостерону утворюється з дегідроепіандростерону в надниркових залозах і яєчниках. У чоловіків з ДГЕА виробляється лише 5% пулу тестостерону, тому це не має клінічного значення. Напрямок метаболізму дегідроепіандростерону залежить насамперед від тканини-мішені й активності ферментів, що каталізують у ній ці зміни, а не від статі.
Біологічні ефекти ДГЕА і ДГЕА-С:
- покращення лібідо та потенції;
- антидепресивна дія;
- стимуляція формування кісткової тканини;
- пригнічення резорбції кісткової тканини;
- стимуляція синтезу колагену в шкірі та білків у міоцитах;
- покращення чутливості до інсуліну;
- зниження концентрації холестерину та пригнічення накопичення ліпідів у інтимі судин;
- судинорозширювальний ефект та модуляція імунної відповіді – збільшення кількості NK-клітин (природні кілери, частина неспецифічного імунітету), зміна активності Т-хелперних лімфоцитів (відповідають за специфічний імунітет).
Основні показання для визначення концентрації дегідроепіандростерону (ДГЕА):
- діагностика синдромів гіперандрогенії;
- діагностика надниркової недостатності.
Катехоламіни
У мозковій речовині надниркових залоз виробляються адреналін і норадреналін, а також невелика кількість дофаміну, що відноситься до катехоламінів.
Адреналін, основний синтезований продукт мозкової речовини надниркових залоз (становить 80% катехоламінів, що виділяються з мозкової речовини надниркових залоз), зберігається ними і секретується у кровообіг головним чином при стресі.
Норадреналін виробляється не лише у мозковій речовині надниркових залоз, а й у постгангліонарних симпатичних волокнах, синтезується з амінокислоти тирозину та перетворюється на адреналін у відповідь на вивільнення кортизолом кори надниркових залоз.
Дофамін, попередник норадреналіну, функціонує головним чином як нейромедіатор у центральній нервовій системі та у менших кількостях виробляється наднирковими залозами й периферичними симпатичними гангліями.
Клітини мозкової речовини надниркових залоз зберігають катехоламіни у цитоплазматичних гранулах, які під впливом ацетилхоліну виділяються у капіляри. Катехоламіни мають різноманітний вплив на обмінні процеси й серцево-судинну систему та виділяються у відповідь на стрес, фізичні навантаження, біль, шок, гіпоглікемію або, наприклад, безпосередньо перед іспитом.
Вони діють швидше ніж кортизол – активація симпатоадреналової системи не регулюється гіпофізом.
Гормони мозкової речовини надниркових залоз діють на мембранні адренорецептори, пов'язані з кількома типами G-білків, впливаючи на різні системи організму людини. Біологічний ефект переданого сигналу залежить від типу рецептора і клітини. Функцію другого месенджера (передавача) виконують іони кальцію (α1-рецептори) або аденілатциклаза (α2 і β-рецептори).
Ефекти стимуляції рецепторів, що належать до різних класів і підтипів, істотно відрізняються. До них відносять, зокрема: підвищення артеріального тиску в результаті вазоконстрикції, вивільнення вільних жирних кислот з жирових клітин, розпад глікогену (резервна речовина), бронходилатацію, пригнічення перистальтики кишківника.
Системні ефекти катехоламінів є результатом дії аміну на щільність окремих рецепторів у деяких органах.
Норадреналін суттєво впливає на α-рецептори, менше – на β1-рецептори, найменше – на β2-рецептори, через що спостерігається підвищення артеріального тиску, прискорення серцевого ритму, зменшення кровотоку через судинне русло шкіри, нирок, печінки та скелетних м’язів.
Адреналін, навпаки, скорочує дрібні артеріоли у шкірі та нирках, але завдяки дії на β2-рецептори розслаблює кровоносні судини скелетних м’язів і печінки та викликає розслаблення мускулатури шлунково-кишкового тракту (окрім сфінктерів), матки при вагітності та бронхів. Адреналін також здійснює численні метаболічні дії, підвищуючи концентрацію глюкози та вільних жирних кислот у крові – важливих субстратів для м’язів у «реакції боротьби або втечі», що виникає під час стресу.
Катехоламіни, які циркулюють у крові у зв’язаному з альбуміном стані, розкладаються у печінці двома ферментами: моноаміноксидазою (МАО) і катехол-орто-метилтрансферазою (КОМТ).
Адреналін і норадреналін є у сироватці крові. Вони виділяються зі сечею у незміненому вигляді та у вигляді метаболітів перетворюються на ванілілмигдальну кислоту (ВМА або ГММА), яка виводиться разом зі сечею. Рівень ВМА вимірюється у сечі для діагностування феохромоцитоми, рідкісної пухлини мозкової речовини надниркових залоз.
Показання до визначення катехоламінів:
- підтвердження або виключення феохромоцитоми, підозрюваної при таких симптомах: пароксизмальна артеріальна гіпертензія, рідше стійка, головні болі, проливний піт, блідість шкіри, ортостатична гіпотензія (раптове зниження артеріального тиску після вертикалізації, тобто зміни положення тіла, наприклад, з лежачого на стояче), біль у животі, нудота, блювання, закреп, безпричинна втрата ваги, аритмії;
- підозра на нейробластому, зокрема у дітей (симптоми: біль у животі, грудях, спині, кістках, безболісні підшкірні вузлики, безпричинна втрата ваги, кашель, задишка, субфебрильна температура);
- оцінка ефективності лікування феохромоцитоми та рецидивів;
- оцінка секреції катехоламінів при нейроендокринних пухлинах та пухлинах надниркових залоз;
- у людей з обтяженим сімейним анамнезом феохромоцитоми;
- огляд та оцінка пацієнтів з порушеннями функцій вегетативної нервової системи та з вегетативною нейропатією.
Порушення роботи надниркових залоз
Порушення функції надниркових залоз полягає у виробленні надлишку гормонів (гіпертиреоз), їхній недостатній функції (гіпотиреоз) або диспропорції між виробленням окремих груп гормонів (блокування ферментів). Причина цих розладів може критися у самих надниркових залозах або бути результатом їхньої аномальної стимуляції.
Чотири найсерйозніші захворювання, пов'язані з гормонами кори надниркових залоз, є відносно рідкісними. До них відносять:
- синдром Кушинга – хронічне, надмірне виділення кортизолу;
- хворобу Кушинга – викликане пухлиною, що виділяє АКТГ;
- синдром Конна – альдостеронсекретуюча пухлина;
- хворобу Аддісона – дефіцит кортизолу та альдостерону.
Синдром Конна та синдром Кушинга є важливими причинами ендокринної гіпертензії.
Надниркова недостатність: причини і діагностика
Адренокортикальна недостатність внаслідок ураження обох нирок виникає, коли руйнується не менше ніж 90% їхньої маси (первинна гіпофункція).
Гіпотиреоз, який розвивається внаслідок відсутності стимулюючої дії АКТГ, є вторинною наднирковою недостатністю, що може бути наслідком ураження гіпофіза (недостатня кількість АКТГ) або гіпоталамуса (відсутність хронічної ниркової недостатності (ХНН) і, як наслідок, АКТГ).
Найчастіше причиною надниркової недостатності є аутоімунний процес, та в окремих випадках (до 10%) захворювання може розвинутися внаслідок пухлинної інфільтрації або туберкульозного процесу.
У діагностиці гіпоадренокортицизму основними дослідженнями є визначення рівня кортизолу та АКТГ у сироватці крові. Визначення рівня кортизолу проводять у ранкові та вечірні години. Водночас визначення концентрації АКТГ слід проводити у стаціонарних умовах через обмеження стабільності параметрів у досліджуваному матеріалі та можливість допущення долабораторної помилки. Візуалізаційні тести дуже важливі для діагностики.
Первинна недостатність кори надниркових залоз (хвороба Аддісона) є рідкісним ендокринним розладом, спричиненим дефіцитом гормонів надниркових залоз.
До неспецифічних симптомів надниркової недостатності відносять:
- слабкість, зниження толерантності до фізичних навантажень;
- втрата апетиту;
- нудота, блювання;
- рідкий стілець;
- біль у м'язах і суглобах;
- непритомність (внаслідок ортостатичної гіпотензії або гіпоглікемії).
Характерні ознаки:
- потемніння шкіри, зокрема у місцях, які піддаються впливу сонячного проміння або тиску;
- коричневе забарвлення шкіри на суглобах пальців, ліній складок на кистях і тильного боку кистей, ареоли сосків, рубці.
Недіагностована первинна надниркова недостатність може призвести до надниркового кризу, що становить загрозу життю.
Гіперадренокортицизм: причини і діагностика
Гіперадренокортицизм у секреції усіх груп гормонів може бути первинним, тобто незалежним від кортикотропіну – АКТГ. Він також може бути результатом пухлини (аденоми, раку) або її росту (гіперплазія) в корі надниркових залоз.
Вторинний гіперадренокортицизм є АКТГ-залежною формою (з гіпофізарним або ектопічним джерелом АКТГ).
Симптоми гіперадренокортицизму:
- центральне ожиріння з накопиченням жиру на обличчі, шиї та надключичних ямках;
- почервоніння обличчя і у ділянці декольте;
- атрофія м'язів плечового і тазового поясів;
- синьо-червоні розтяжки (стрії) на шкірі живота, сідниць, іноді кінцівок;
- ламкість судин – легке утворення синців;
- суха, тонка, схожа на пергамент шкіра – легко пошкоджується, рани вкрай важко загоюються;
- грибкові ураження (зокрема, поширений лишай) і гнійні ураження (фурункули);
- ослаблений імунітет (можуть розвинутися дуже важкі бактеріальні й вірусні інфекції та генералізовані грибкові інфекції);
- численні порушення обміну речовин.
Пацієнти зі синдромом Кушинга (рідкісне захворювання, спричинене хронічним надлишком глюкокортикоїдів) можуть відчувати:
- інсулінорезистентність, схильність до гіперглікемії;
- непереносимість глюкози;
- діабет ІІ типу;
- гіперхолестеринемія та гіпертригліцеридемія;
- підвищений рівень сечової кислоти;
- гіперемію і тромбоцитемію (підвищений ризик утворення тромбів);
- підвищення артеріального тиску;
- схильність до гіпокаліємії (зниження рівня калію);
- ослаблення міцності кісток і можливість патологічних переломів;
- гіперкальціурію – ризик утворення каменів у нирках;
- зміни очного дна – судинні зміни, викликані гіпертонією і цукровим діабетом;
- підвищення внутрішньоочного тиску і катаракта;
- розлади пам'яті та когнітивні функції;
- безсоння;
- порушення менструального циклу або вторинну аменорею у жінок;
- еректильну дисфункція (у чоловіків);
- зниження лібідо у людей обох статей.
Гіперкортизолемія може викликати психічні розлади: часто це депресивні стани, але при синдромі Кушинга також можливі важкі постстероїдні психози.
При підозрі на гіперкортицизм найпростішим скринінговим тестом, який можна провести амбулаторно, є тест гальмування з одноразовим введенням 1 мг дексаметазону о 23:00.
Доцільно також визначити добовий ритм секреції кортизолу. Наступним етапом діагностики є визначення ранкової концентрації кортикотропіну АКТГ, яке через обмежену стабільність показника у досліджуваному матеріалі та можливістю допущення долабораторної помилки необхідно проводити в умовах стаціонару або ж матеріал для дослідження необхідно забирати у пунктах відбору проб у лабораторії.
Хвороба Кушинга
Хвороба Кушинга пов’язана зі специфічним надлишком глюкокортикоїдів, викликаним аденомою гіпофіза і гіперплазією надниркових залоз (стимуляція кори надниркових залоз гіпофізом – у клітинах аденоми зникає зворотний зв'язок, що пригнічує надмірну секрецію АКТГ).
Синдром Кушинга пов’язують з додатковим посиленням пігментації шкіри, а лікування хвороби передбачає хірургічне видалення аденоми.